DATE2026.04.22 #Press Releases
柔軟性、正確性、送達性、編集効率に優れた万能のゲノム編集ツールの開発に成功
発表のポイント
- 小型SaCas9の改変体、eSaCas9-NNGの開発に成功しました。
- eSaCas9-NNGは広い標的可能範囲、高い標的特異性、小型な遺伝子サイズ、高い活性という四つの性能指標に優れています。
- eSaCas9-NNGを技術基盤とした次世代型の遺伝子治療の開発が期待されます。

分子改変によって得られたeSaCas9-NNG
概要
東京大学大学院理学系研究科の大村紗登士助教、仲川綾哉大学院生(研究当時)、梶本祥平大学院生(研究当時)、濡木理教授と、同大学先端科学技術研究センターの西増弘志教授らによる研究グループは、ゲノム編集ツールとして利用されているStaphylococcus aureus(黄色ブドウ球菌)(注1)に由来する小型SaCas9に12個のアミノ酸変異(注2)を導入し、SaCas9の高機能改変体eSaCas9-NNG(注3)を開発しました。eSaCas9-NNGは広い標的可能範囲・高い標的特異性・小型サイズ・高い活性という、ゲノム編集ツールに求められる四つの性能指標を同時に実現しています。さらに研究グループは、クライオ電子顕微鏡(注4)を用いてeSaCas9-NNGの活性化機構の詳細を解明しました。本成果は、eSaCas9-NNGを技術基盤とした高精度かつ安全性の高い次世代遺伝子治療技術の実現に貢献することが期待されます。
発表内容
原核生物のCRISPR-Cas獲得免疫機構に関与するCas9は、ガイドRNAと複合体を形成し、ガイドRNAのガイド配列と相補的で、かつ近傍にPAM(protospacer adjacent motif)(注5)と呼ばれる特定の塩基配列を有する二本鎖DNAを切断する「はさみ」として機能します。ガイド配列は任意の配列に設計可能なため、Cas9は生命の設計図であるゲノム情報を人為的に書き換えられるゲノム編集技術として、基礎研究、農作物の品種改良、遺伝子治療などにおいて広く利用されてきました。
現在、生体内における活性の高さからStreptococcus pyogenes由来SpCas9がゲノム編集ツールとして最も広く利用されています。しかしながらSpCas9によるゲノム編集は、①標的とするDNA配列近傍に「GG」という2塩基からなるPAM配列を必要とするため、標的可能なゲノム領域が制限されること、②ガイド配列と標的DNAとの間の数塩基のミスマッチを許容する性質に起因して、意図しないDNA切断(オフターゲット効果)が生じうること、③遺伝子サイズが大きく、標的組織への送達効率に課題があること、という問題点が指摘されています(図1)。近年①のPAMによる標的可能範囲の制限を克服した、より短いPAM配列を認識するCas9改変体が盛んに開発されてきましたが、PAMの短縮化はオフターゲットの増加につながるというジレンマを抱えています。

図1:Cas9を用いたゲノム編集における問題点
(実験医学増刊:「構造生命科学 AlphaFold時代にどう活かす?」より引用)
今回、東京大学の濡木理教授らの研究グループは、SpCas9よりも遺伝子サイズが1 kb以上小型なStaphylococcus aureus由来SaCas9に着目しました。野生型SaCas9はNNGRRT (Nは任意の塩基、RはAまたはG)という比較的長いPAMを認識し、ガイド配列の末端付近に生じるミスマッチを許容しやすい性質を有しています。研究グループは、このSaCas9の立体構造情報に基づいて合理的な分子改変を施すことで、PAMとしてGを含むNNG配列(NNG)を認識し、かつオフターゲット効果を抑制した改変体 eSaCas9-NNG の開発に成功しました(図2A)。
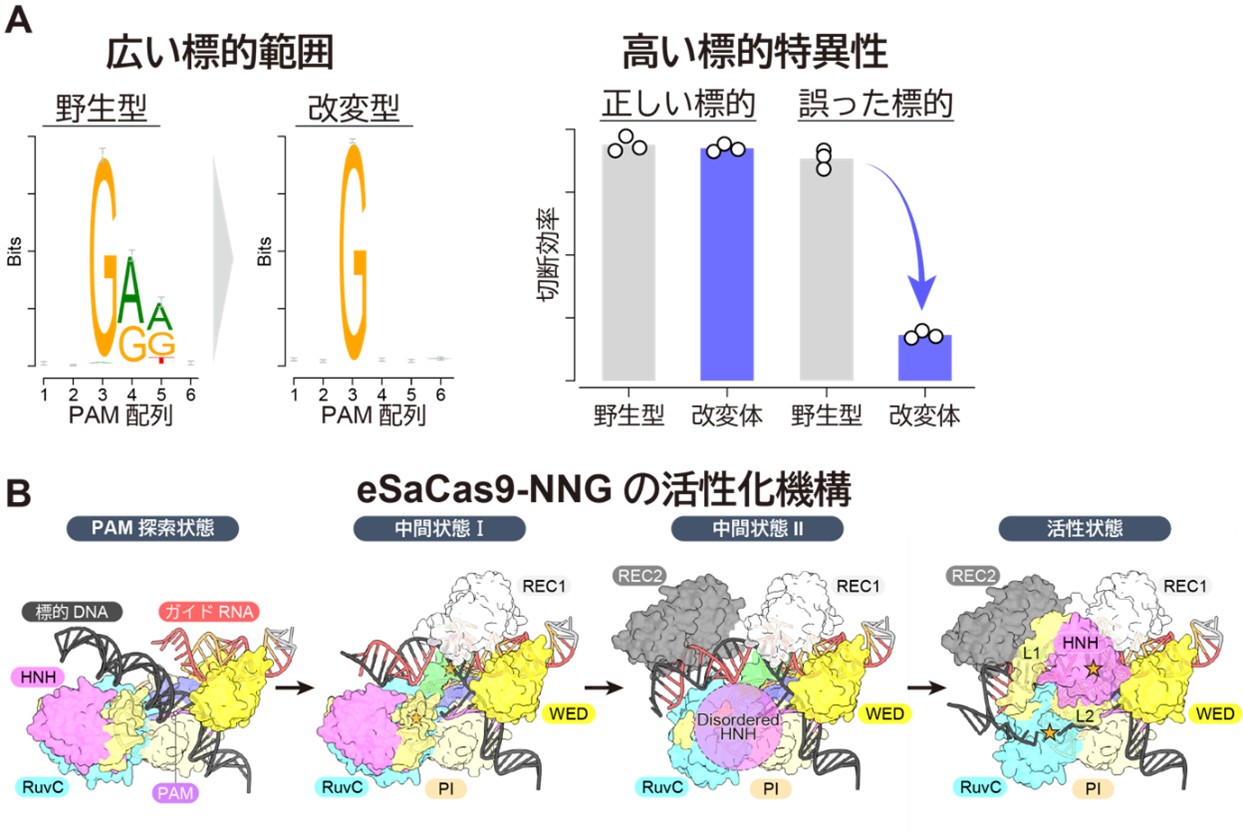
図2:eSaCas9-NNGの特性と活性化機構
eSaCas9-NNGは、野生型SpCas9やSaCas9では標的とすることができないDNA配列に対して、哺乳類培養細胞およびマウス個体において高いDNA切断活性を示し、小型、広い標的可能範囲、高い標的特異性を兼ね備えた高性能なゲノム編集ツールとしての有用性が示されました。さらに研究グループは、クライオ電子顕微鏡解析によりeSaCas9-NNGが標的DNAを切断する過程における複数の状態の立体構造を決定しました(図2B)。その結果、eSaCas9-NNGによる標的可能範囲の拡大および高い標的特異性を実現する構造基盤に加え、DNA切断に至る段階的な活性化機構が明らかになりました。本成果は、eSaCas9-NNGを技術基盤とした高精度かつ安全性の高い次世代遺伝子治療技術の実現に貢献することが期待されます。
発表者・研究者等情報
東京大学
大学院理学系研究科 生物科学専攻
濡木 理 教授
大村 紗登士 助教
仲川 綾哉 博士課程学生(研究当時)
梶本 祥平 修士課程学生(研究当時)
先端科学技術研究センター
西増 弘志 教授
兼:大学院工学系研究科化学生命工学専攻
論文情報
-
雑誌名 Nature Communications 論文タイトル Engineering a compact high-fidelity Staphylococcus aureus Cas9 variant with broader targeting range and mechanistic insights into its activation著者 Satoshi N. Omura, Ryoya Nakagawa, Shohei Kajimoto, Sae Okazaki, Soh Ishiguro, Hideto Mori, Yuji Kashiwakura, Takafumi Hiramoto, Kio Horinaka, Mamoru Tanaka, Hisato Hirano, Kasey Jividen, Keitaro Yamashita, Shengdar Q. Tsai, Nozomu Yachie, Tsukasa Ohmori, Hiroshi Nishimasu*, and Osamu Nureki* (*責任著者) DOI番号 10.1038/s41467-026-71626-2
研究助成
本研究は、国立研究開発法人日本医療研究開発機構(AMED)「創薬等ライフサイエンス研究支援基盤事業」の一環とした「創薬等先端技術支援基盤プラットフォーム(BINDS)」 (課題番号:JP25ama121012)、AMED「エイズ対策実用化研究事業」 (課題番号:JP25fk0410061 研究分担者:濡木 理)、AMED「再生・細胞医療・遺伝子治療実現加速化プログラム」 (課題番号:23bm1123039h000125bm1223004h0003, 25bm1123046h0003 研究分担者:濡木 理)などの支援により行われました。
用語解説
注1 Staphylococcus aureus(黄色ブドウ球菌)
細菌の一種。食中毒などのヒトの病気の原因になる。↑
注2 12個のアミノ酸変異
タンパク質は複数のアミノ酸が連なった構成されている。SaCas9は1053個のアミノ酸が連なって形成されるが、今回我々はそのうち12個のアミノ酸に変異を導入した。↑
注3 eSaCas9-NNG
SaCas9の改変体。Enhanced-specificity SaCas9-NNG (eSaCas9-NNG)の略称。↑
注4 クライオ電子顕微鏡
液体窒素(-196℃)冷却下でタンパク質などの分子に対して電子線を照射し、試料の観察を行うための装置。タンパク質や核酸の立体構造の決定に利用されている。↑
注5 PAM(protospacer adjacent motif)
Casタンパク質がDNAに結合するために必要な特定のDNA配列。↑


