DATE2025.07.19 #Press Releases
“天然物骨格リデザイン”が切り拓く中分子創薬
ー抗がん剤エクテナサイジンの再設計によるマクロ環状中分子群の創製ー
発表のポイント
- 抗がん剤エクテナサイジン743(トラベクテジン)の骨格を戦略的に再設計し、14〜17員環の多様なマクロ環状中分子群を、従来法の約半分にあたる6〜10段階で合成する革新的な手法を確立しました。
- 得られた中分子群はDNA切断活性を保持しつつ、各種がん細胞株に対して極めて強力な増殖抑制効果を示し、マクロ環構造の差異に応じて活性プロファイルが変化することも明らかにしました。
- 構造・機能・合成容易性の最適化を実現する“天然物骨格リデザイン”の有効性を実証し、中分子創薬の新しいアプローチとして次世代抗がん剤開発への貢献が期待されます。
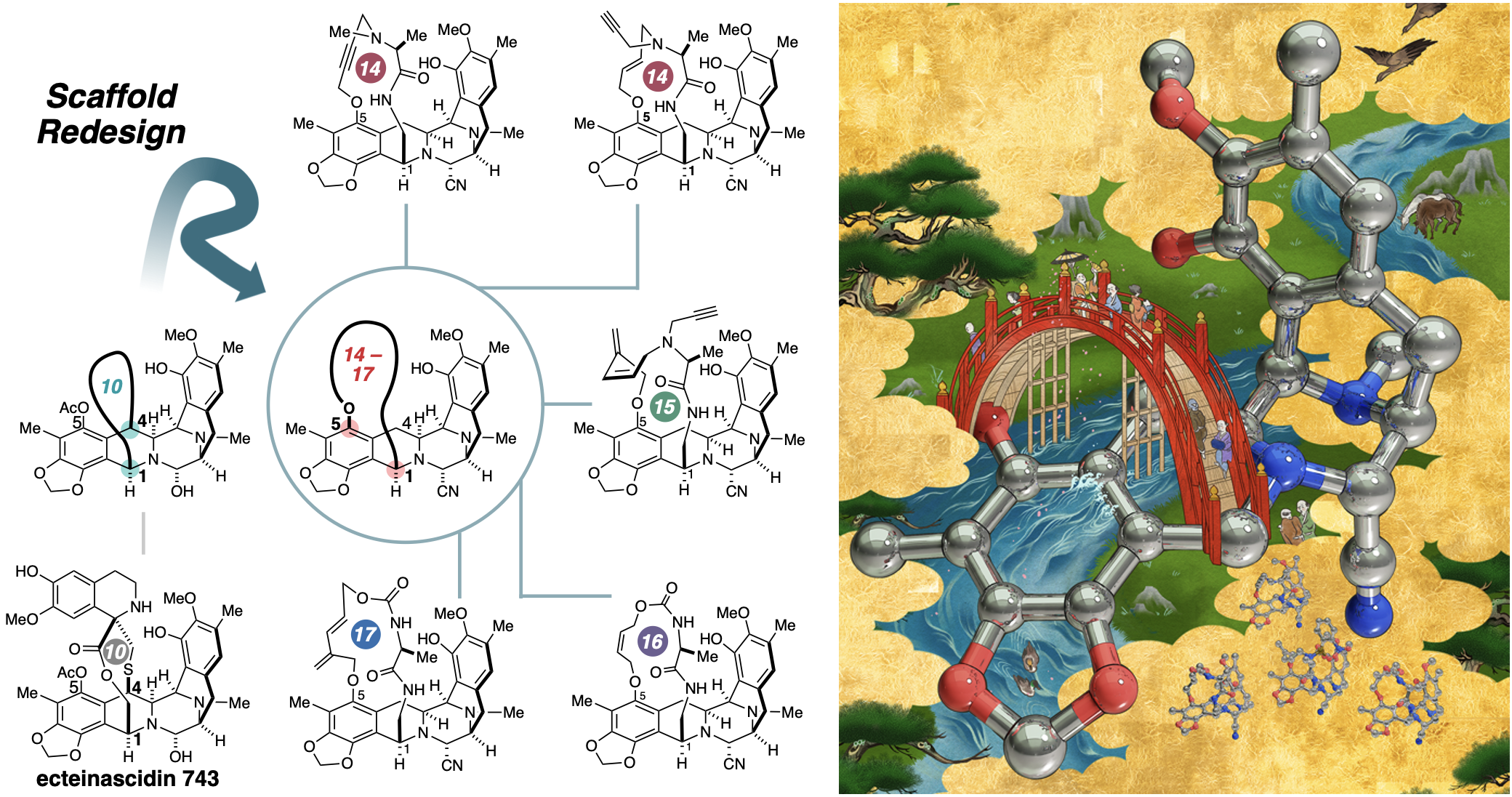
天然物骨格のリデザイン戦略による抗腫瘍性マクロ環状中分子群の創製
発表概要
東京大学大学院理学系研究科の谷藤涼助教、細野絵里奈氏(研究当時:修士課程)、鎌倉寿恵氏(研究当時:技術補佐員)、大栗博毅教授は、東京大学大学院工学系研究科の吉田知史大学院生、佐藤宗太特任教授、公益財団法人がん研究会がん化学療法センター分子生物治療研究部の村松由起子主任研究助手、清宮啓之部長、同センター分子薬理部の大橋愛美嘱託研究助手、旦慎吾部長らと共同で、海洋天然物(注1) 由来のエクテナサイジン743(トラベクテジン、注2 )の骨格構造を戦略的に再設計し、構造多様性と強力な抗腫瘍活性を両立する10種類以上のマクロ環状中分子(注3 、注4 )を短工程で創製する合成プロセスを開発しました。得られた誘導体群はDNA二重鎖切断(注5) を誘導する活性を保持しながら、39種のヒトがん細胞株(JFCR39、注6 )の増殖をサブナノモル濃度で強力に抑制しました。さらに、マクロ環構造の違いにより、各種がん細胞に対する活性プロファイルが大きく変化することも明らかとなり、入手困難な天然物を基盤とした抗がん剤開発における分子設計の新たな指針となることが期待されます。
発表内容
天然物の分子骨格は、生体適合性や生体分子に対する高い親和性を備える一方で、その構造が極めて複雑かつ合成困難であることから、医薬品としての実用化には依然として多くの課題が存在します。海洋天然物エクテナサイジン743(トラベクテジン)は、優れた抗腫瘍活性を示し、悪性軟部腫瘍の治療薬として臨床応用されています(図1)。また、その合成誘導体であるルルビネクテジンは、小細胞肺がん治療薬として実用化されており、天然物を基盤とした中分子抗がん剤開発の成功例として知られています。しかし、これらの化合物の供給には、21段階に及ぶ煩雑な半合成プロセスが必要とされてきました。
本研究では、こうした合成上の課題を克服するため、エクテナサイジン743の分子構造を戦略的に再設計し、より簡便かつ柔軟に誘導体を創製可能な新たな合成戦略を開発しました。DNAアルキル化活性を担う6環性母骨格を保持しながら、マクロ環の橋かけ位置を従来のC1-C4位からC1-C5位へと改変する“骨格リデザイン戦略”を導入することで、14〜17員環のマクロ環ユニットを有する16種の新規化合物をわずか6〜10段階で迅速に合成することに成功しました。

図1:エクテナサイジン743 骨格リデザイン戦略。
本戦略では、エクテナサイジン743のC5位フェノール性水酸基を新たな架橋点とし、共通の環化前駆体から銅触媒によるA3カップリング(注7) 、およびルテニウム触媒による閉環メタセシス反応(注8) で14~17員環のマクロ環状誘導体を短段階で合成しました(図2)。各化合物についてX線結晶構造(注9) を取得し、マクロ環構造を段階的に拡張しながら系統的な構造多様化が達成されていることを実証しました。

図2 :設計中分子群の合成戦略とX線結晶構造。
マクロ環構造の拡張と構造多様化。16員環化合物の立体構造は大型放射光施設SPring-8(注10) BL26B1ビームラインで得られた回折データを用いて解明。
エクテナサイジン743におけるマクロ環は、DNA修復酵素の機能を阻害して抗腫瘍活性を発揮する上で重要な構造要素とされています。本研究では、その機能を保持したまま構造多様化を実現し、圧倒的に短い工程数で合成できる新しい誘導体群の創出に成功しました。さらに、計算化学的に最適化した構造の重ね合わせから、従来のC1-C4架橋骨格では到達困難であった新たなケミカルスペースへのアクセスが可能であることを示しました(図3)。

図3 :(左)マクロ環を修飾した合成中分子群。X線結晶構造は大型放射光施設SPring-8 BL26B1ビームラインで得られた回折データを用いて解明。(右)計算化学的に最適化した構造の重ね合わせ。灰色はエクテナサイジン743を示す。新規誘導体群は未踏のケミカルスペース (–x, y, z象限) への拡張を達成。
代表的な誘導体群についてがん細胞内での作用を評価した結果、エクテナサイジン743と同様に、リデザイン骨格を有する中分子群もγ-H2AX(注11) および53BP1(注12) の集積を誘導し、DNA二重鎖切断を引き起こすことが確認されました(図4)。この結果は、マクロ環ユニットの大胆な構造改変にもかかわらず、がん細胞内における特異的なDNA切断機能が保持されていることを明確に示しています。

図4 :がん細胞内におけるDNA二重鎖切断の可視化。
緑色(γ-H2AX)と赤色(53BP1)のシグナルが重なった黄色の輝点が、DNA二重鎖切断の発生部位を示す。青色は細胞核を示す。リデザインした中分子群も細胞核に到達し、エクテナサイジン743と同様にDNA二重鎖切断を誘導することが確認された。
39種のヒトがん細胞株パネル(JFCR39)を用いた活性評価の結果、各誘導体はいずれもサブナノモル濃度で強力な細胞増殖阻害活性を示しました(図5)。特に、マクロ環のサイズや立体化学といった構造上のわずかな違いにより、がん細胞ごとの感受性パターンに顕著な違いが生じ、活性プロファイルに明確な変化が認められました。この結果は、マクロ環骨格のリデザインによって、がん種ごとに選択性を付与できる抗がん剤の創製が可能であることを示唆しています。

図5:JFCR39がん細胞パネルを用いた中分子誘導体群の増殖阻害活性評価。
50%増殖阻害濃度 (GI50、注13 ) の値が低いほど、がん細胞に対する増殖抑制効果が高いことを示す。14・15員環誘導体はエクテナサイジン743と類似した作用プロファイルを示したのに対し、16・17員環化合物はエキノマイシンとの類似性が示唆された。
本研究は、天然物の複雑な分子骨格を戦略的に再設計する“天然物骨格リデザイン”の有効性を実証し、中分子創薬における構造多様性の拡張と生物活性の最適化を両立させる新たな設計指針を提示するものです。本成果は、天然物由来の医薬シーズの再構築と機能拡張に向けた革新的アプローチであり、次世代抗がん剤の分子設計における新たな羅針盤となることが期待されます。
発表者・研究者等情報
東京大学
大学院理学系研究科
谷藤 涼 助教
細野 絵里奈 研究当時:修士課程
鎌倉 寿恵 研究当時:技術補佐員
大栗 博毅 教授
大学院工学系研究科
吉田 知史 博士課程
佐藤 宗太 特任教授 兼:分子科学研究所 客員教授
がん研究会 がん化学療法センター
分子生物治療研究部
村松 由起子 主任研究助手
清宮 啓之 部長
分子薬理部
大橋 愛美 嘱託研究助手
旦 慎吾 部長
関連リンク
論文情報
-
雑誌名 Chem 論文タイトル Strategic Scaffold Redesign of Ecteinascidins: An Approach for Generating Anticancer Macrocycles著者 Ryo Tanifuji,* Erina Hosono, Hisae Kamakura, Yukiko Muramatsu, Satoshi Yoshida, Sota Sato, Yoshimi Ohashi, Shingo Dan,* Hiroyuki Seimiya,* Hiroki Oguri*
(*責任著者)DOI番号 10.1016/j.chempr.2025.102664
研究助成
本研究は、以下の助成金によって実施されました。
・JSPS科研費(JP22K14790, JP22H00346, JP22H05127, JP24K08726)
・AMED SCARDA 世界トップレベルワクチン研究開発拠点形成プログラムUTOPIA(JP223fa627001)
・JST ACT-X(JPMJAX211A)
・内藤記念科学研究助成金
・旭硝子財団研究助成金
・日本財団 助成金
また、JFCR39パネルによる薬効評価は、先端モデル動物支援プラットフォーム(AdAMS)・分子プロファイリング支援活動(JP22H04922)による支援をうけて実施されたものです。
用語解説
注1 天然物
自然界に存在し、生物(微生物・植物・海洋生物など)によって産生される分子群。特有の立体構造や高い生理活性を有し、医薬品のリード化合物や創薬シーズとして重要視されている。↑
注2 エクテナサイジン743(トラベクテジン)
カリブ海産ホヤ由来の海洋天然物で、DNAに共有結合し、さらにDNA修復タンパク質を阻害して抗腫瘍活性を発揮する。悪性軟部腫瘍の治療薬トラベクテジンとして臨床使用されている。↑
注3 マクロ環
10個以上の原子で構成される大きな環状構造。構造の柔軟性と多様性を兼ね備えていることから、中分子創薬における有望な骨格として注目されている。↑
注4 中分子
分子量約500~2000程度の化合物。低分子薬と高分子薬の中間的特性を持ち、細胞膜透過性と標的選択性を兼ね備える創薬モダリティ。↑
注5 DNA二重鎖切断
DNAの両鎖が同時に切断された状態。細胞にとって致命的な損傷であり、修復されなければ細胞死を引き起こす。がん細胞選択的に誘導することで、抗がん剤の有効な作用機序となり得る。↑
注6 JFCR39
公益財団法人がん研究会が整備した39種類のヒトがん細胞株パネル。がんの組織起源や薬剤感受性が異なる細胞株で構成され、抗がん剤候補の活性スペクトルから作用機序の解析を可能とする評価系。↑
注7 A3カップリング
アルデヒド、アルキン、アミンの三成分を銅触媒下で連結する多成分連結反応。複雑な構造の簡便な合成が可能となる。↑
注8 閉環メタセシス反応
ルテニウムなどの金属触媒を用いてオレフィンやアセチレンを連結し、炭素-炭素結合を形成することで、環状化合物を合成する反応。複雑な環状構造の構築に広く利用される。↑
注9 X線結晶構造
結晶化した化合物にX線を照射し、得られた回折パターンを解析することで、原子の三次元配置を高精度に可視化した構造情報。分子構造の証明や立体配座の検証に広く利用される。↑
注10 SPring-8
兵庫県に設置された大型放射光施設。世界最高水準の高輝度・高指向性の放射光を利用でき、化合物の結晶構造や物性の高精度な解析を実現する。↑
注11 γ-H2AX(ガンマエイチツーエーエックス)
DNA二重鎖切断時にヒストンH2AXのセリン139位がリン酸化されたマーカー。DNA損傷応答の初期指標として用いられる。↑
注12 53BP1(フィフティスリービーピーワン)
DNAの損傷部位に集まるタンパク質の一つで、γ-H2AXとともに細胞のDNA損傷応答に関与する。損傷箇所の修復を促進する役割を担っている。↑
注13 50% 増殖阻害濃度(GI50)
化合物の細胞増殖阻害活性を評価する指標。一定時間内に無処理で増殖した細胞数を100%としたとき、化合物処理によって増殖が50%に抑えられる濃度を表す。値が小さいほど細胞増殖阻害活性が強いことを示す。↑


