DATE2023.08.24 #Press Releases
金属イオンでDNA鎖置換反応を引き起こす
――DNA分子機械の開発やDNA分子コンピューティングへの応用に期待――
竹澤 悠典(化学専攻 助教)
森 圭太(化学専攻 日本学術振興会特別研究員:研究当時)
黄 薇恩(化学科学部4年生:研究当時)
西山 康太郎(化学専攻 博士課程:研究当時)
邢 瞳(修士課程:研究当時)
中間 貴寛(化学専攻 博士課程:研究当時)
塩谷 光彦(化学専攻 教授)
発表のポイント
- 修飾核酸塩基である5-ヒドロキシウラシル塩基を導入したDNA鎖を用いて、ガドリニウム(GdIII)イオンの添加・除去によりDNA鎖置換反応を引き起こすことに成功した。
- さらに、GdIIIイオンに応答して開閉するDNA分子ピンセット構造や、触媒活性を制御できるデオキシリボザイム(DNAzyme)の開発に成功した。
- 本研究成果は、金属イオンを外部刺激として駆動するDNA分子機械の開発や、DNA分子コンピューティングへの応用が期待される。
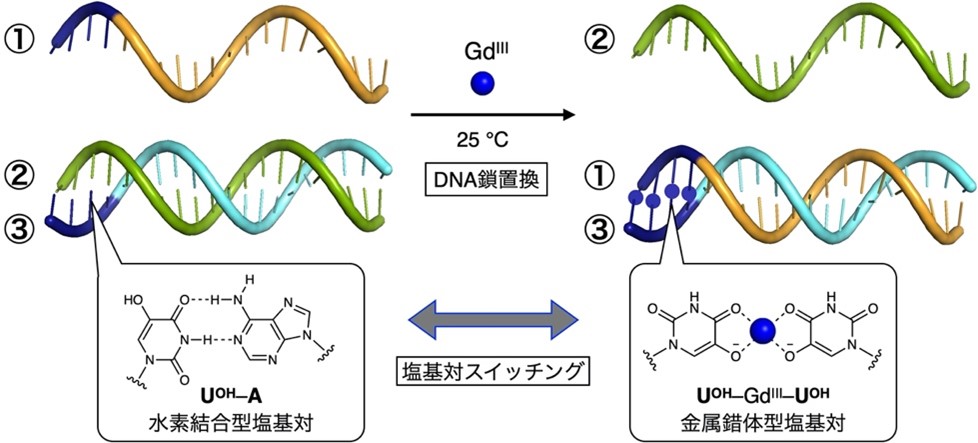
ガドリニウムイオン(GdIII)の添加により引き起こされるDNA鎖置換反応
発表概要
東京大学大学院理学系研究科の塩谷光彦教授と竹澤悠典助教らによる研究グループは、修飾核酸塩基である5-ヒドロキシウラシル(UOH)塩基(注1)を導入したDNA鎖を用いて、ガドリニウムイオン(GdIII)(注2)の添加・除去によりDNA鎖置換反応(注3)を引き起こすことに成功しました。
近年、DNA分子が塩基配列に応じて二重鎖を形成する性質を利用して、さまざまなナノ構造体や機能性分子を作るDNAナノテクノロジー(注4)の研究が盛んになっています。なかでもDNA鎖置換反応は、入力となる一本鎖DNAの結合によりDNA二重鎖の組み換えが起こる反応で、DNA分子機械(注5)やDNA分子演算回路(注6)の開発など、動的DNAナノテクノロジーにおける基盤技術として注目されています。
本研究では、5-ヒドロキシウラシル(UOH)塩基が、天然塩基対に類似した水素結合型塩基対(UOH–A)だけでなく、GdIIIイオンとの配位結合を介した金属錯体型塩基対(注7)(UOH–GdIII–UOH)を形成することを利用して、金属イオンを外部刺激としたDNA鎖置換反応を実現しました。さらに、水素結合型塩基対・金属錯体型塩基対の間のスイッチングを活用して、GdIIIイオンに応答して開閉するDNA分子ピンセット構造(注8)や、触媒活性を制御できるデオキシリボザイム(DNAzyme)(注9)を開発しました。本研究成果は、金属イオンを外部刺激として駆動するDNA分子機械の開発や、DNA分子コンピューティングへの応用が期待されます。
発表内容
DNA分子はA–T, G–Cといった塩基対の形成により、塩基配列特異的に会合して二重らせん構造を形成します。これは、塩基配列をうまく設計することでさまざまな集合構造を構築できることを示唆しています。DNA分子の自己集合によりさまざまなナノ構造体や分子デバイスを作る研究は「DNAナノテクノロジー」とも呼ばれており、急速に研究が発展している分野です。なかでもDNA鎖置換反応は、入力となる一本鎖DNAの結合によりDNA二重鎖の組み換えが起こる反応で、DNA分子機械やDNA分子演算回路の開発など、動的DNAナノテクノロジーにおける基盤技術として注目されています。DNAナノテクノロジーをさまざまな化学環境で応用するうえで、DNA/RNA分子以外の刺激により引き起こされるDNA鎖置換反応の開発が重要な課題となっていました。
そこで本研究では、5-ヒドロキシウラシル(UOH)塩基という修飾核酸塩基に着目しました。UOHは天然のチミン(T)塩基と同様に、アデニン(A)塩基と水素結合を介した塩基対(UOH–A)を形成します。一方で、ガドリニウムイオン(GdIII)などの特定の金属イオンの存在下では、金属配位結合を介した金属錯体型塩基対(UOH–GdIII–UOH)を形成することを、当研究グループは報告してきました(Chem. Eur. J., 2015)。そこで、GdIIIイオンの添加・除去により、水素結合型(UOH–A)塩基対と金属錯体型UOH–GdIII–UOH塩基対との間のスイッチングを行うことで、金属イオンを外部刺激としたDNA鎖置換反応を引き起こすことを考えました(図1)。
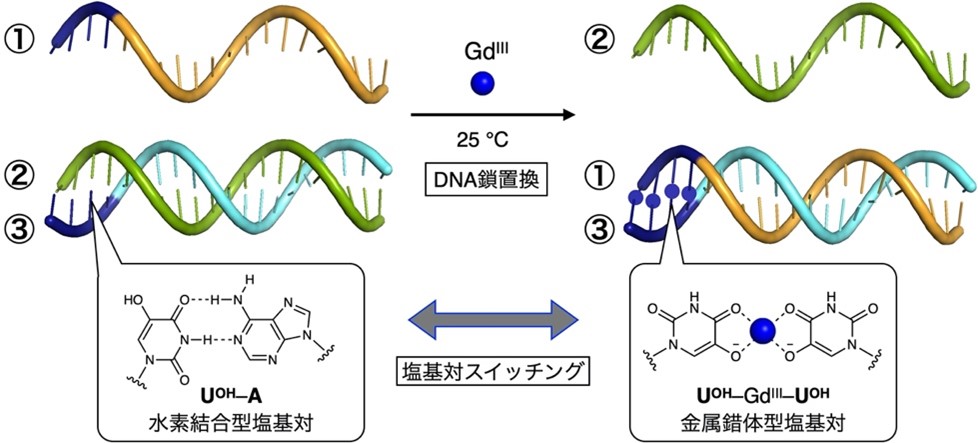
図1:GdIIIイオンの添加により引き起こされるDNA鎖置換反応
はじめは水素結合型塩基対(UOH–A)により②と③が二重鎖を形成しているが、GdIIIイオンを加えると、金属錯体型塩基対(UOH–GdIII–UOH)の形成により①と③が二重鎖を形成するようになる。簡略化のため、GdIIIイオンに結合しているその他の分子(配位子)は省略してある。
末端に連続した4個のUOH塩基を含むDNA鎖③、その相補配列(注10)の天然DNA鎖②、および末端に4個のUOH塩基を含む以外は②と同じ塩基配列のDNA鎖①を用いました。はじめは、水素結合型塩基対(UOH–A)の形成により、②と③が二重鎖を形成します。ここにGdIIIイオンを加えると、金属錯体型塩基対(UOH–GdIII–UOH)の形成により、①と③が二重鎖を形成するようになりました。すなわち、GdIIIイオンの添加により、①が結合し②が放出されるというDNA鎖の置換が起こることを見出しました。また、キレート試薬によりGdIIIイオンを取り除くことにより、逆方向の鎖置換反応が進むことも示されました。以上により、UOH塩基を用いることで、GdIIIイオンに応答する可逆なDNA鎖置換反応を実現できました。
続いて、金属イオンの添加・除去による「水素結合型塩基対(UOH–A)⇔ 金属錯体型塩基対(UOH–GdIII–UOH)」のスイッチングを活用して、GdIIIイオンに応答して開閉するDNA分子ピンセット構造を構築しました(図2)。3本のDNA鎖(a, b, c)からなるピンセット状構造体に対して、UOH塩基を含むDNA鎖(d)をストッパーとして用いました。GdIIIイオンを加えないときは、複数のUOH–A塩基対を介してストッパー鎖(d)が結合することにより、分子ピンセットは閉じた構造となりました。一方、GdIIIイオンを添加するとストッパー鎖(d)が解離して、開いた構造になることがわかりました。キレート試薬を使ってGdIIIイオンの添加と除去を繰り返すことで、DNA分子ピンセットの開閉を4回繰り返すことができました。
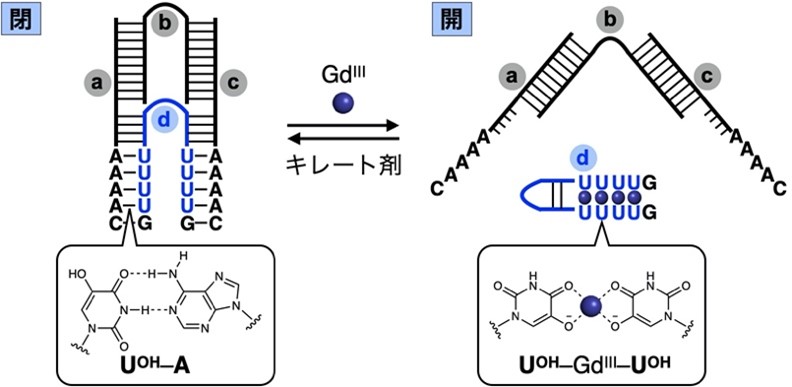
図2:GdIIIイオンの添加・除去により開閉するDNA分子ピンセット構造
GdIIIイオン非存在下では、UOH–A塩基対を介してストッパー鎖(d)が結合して閉じた構造(左)となる。GdIIIイオンを加えるとストッパー鎖(d)が解離し、開いた構造(右)へと変化する。キレート試薬によりGdIIIイオンを除去することで、再び閉じた構造(左)に戻る。
また、触媒活性をもつDNA鎖であるデオキシリボザイム(DNAzyme)の配列中にUOH塩基を導入することにより、金属イオンに応答して活性が制御されるDNAzymeを作ることにも成功しました(図3)。具体的には、RNA切断反応を触媒する既存のDNAzymeをもとに、GdIIIイオン非存在下ではUOH–A塩基対の形成により不活性構造となり、GdIIIイオン存在下ではUOH–GdIII–UOH塩基対の形成により活性構造となるように塩基配列を設計しました。実際にUOH修飾DNAzymeのRNA切断活性を評価したところ、GdIIIイオンの添加により活性が約14倍上昇することが明らかとなりました。さらに、反応中にGdIIIイオンを加えたり、キレート試薬によりGdIIIイオンを除去することにより、DNAzymeの活性の可逆な制御にも成功しました。
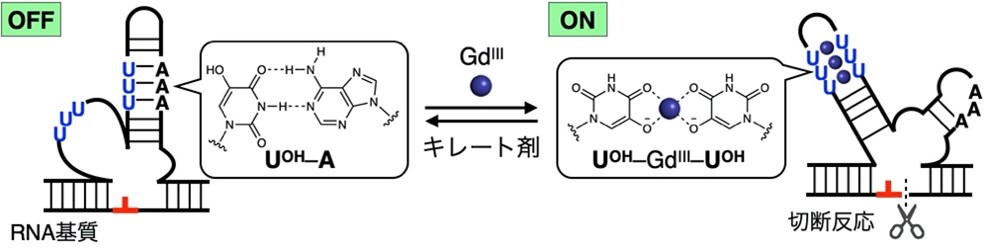
図3:GdIIIイオンの添加・除去により活性を制御できるデオキシリボザイム(DNAzyme)
GdIIIイオン非存在下ではUOH–A塩基対を含む不活性構造(左)となり、GdIIIイオンを加えると金属錯体型塩基対(UOH–GdIII–UOH)の形成により活性構造(右)へと変化する。それにより、GdIIIイオンの添加・除去によるDNAzymeのRNA切断活性制御が可能となった。
このように本研究では、UOH塩基を新しい「部品」として使うことで、GdIIIイオンを外部刺激として構造や活性を制御できるDNA分子システムを設計できることを示しました。本研究で示した方法論は、5-ヒドロキシウラシル(UOH)だけでなく、金属錯体型塩基対を形成する他の種類の修飾核酸塩基にも応用できると期待され、用いる金属イオンの種類も拡張できると考えられます。DNA鎖置換反応は、DNA構造体の動的挙動の誘起やDNAを使った情報伝達・分子演算に応用されていることから、金属イオンを外部刺激として駆動するDNA分子機械の開発やDNA分子コンピューティングへの応用が期待されます。
論文情報
-
雑誌名 Nature Communications 論文タイトル Metal-mediated DNA strand displacement and molecular device operations based on base-pair switching of 5-hydroxyuracil nucleobases著者 Yusuke Takezawa*, Keita Mori, Wei-En Huang, Kotaro Nishiyama, Tong Xing, Takahiro Nakama & Mitsuhiko Shionoya*DOI番号
研究助成
本研究は、科研費「基盤研究(B)(課題番号:JP18H02081およびJP21H02055)」、「挑戦的研究(萌芽)(課題番号:JP22K19100)」、「新学術領域研究 発動分子科学 公募研究(課題番号:JP21H00384)」、「学術変革領域研究(A) 分子サイバネティクス 公募研究(課題番号:JP21H05866およびJP23H04399)」、「特別研究員奨励費(課題番号:JP21J11325)」、「基盤研究(S)(課題番号:JP21H05022)」、「新学術領域研究 配位アシンメトリ 計画研究(課題番号:JP16H06509)」の支援により実施されました。
用語解説
注1 5-ヒドロキシウラシル(UOH)
天然の核酸塩基の一つであるチミン(T)のメチル基(–CH3)が水酸基(–OH)に置き換わった構造の修飾核酸塩基。シトシン(C)塩基が損傷を受けると生成することがある。↑
注2 ガドリニウムイオン(GdIII)
ランタノイドに属する原子番号64の元素・ガドリニウム(Gd)の陽イオン。磁性材料やMRI造影剤に用いられることでも知られる。↑
注3 DNA鎖置換反応
入力となる一本鎖DNAの結合により、DNA二重鎖の組み換えが起こる反応。一般的には、トーホールドと呼ばれる一本鎖部分への入力DNA鎖の結合により開始する。後述するDNA分子機械や演算回路の開発における基本技術である。↑
注4 DNAナノテクノロジー
DNA鎖の配列特異的な会合・自己集合に基づいて、さまざまなナノスケールの構造体や機能分子をボトムアップで構築する研究分野の総称。1980年代に米・ニューヨーク大学のSeemanにより提唱され、特に21世紀に入ってからDNAオリガミ法をはじめ爆発的な進展を見せている。DNA鎖の会合・解離を利用して分子機械や分子演算などへの応用を目指す研究は、動的DNAナノテクノロジーとも呼ばれる。↑
注5 DNA分子機械
機械的な動きを示すDNAナノ構造体のこと。2016年のノーベル化学賞が「分子機械の設計と合成」に与えられたが、DNAを素材として分子機械を構築する研究も盛んである。“伸縮”や“開閉”といった構造変換をするものから、“足場”上を移動したり“荷物”を運んだりするものまで、多様なDNA分子機械が報告されている。 ↑
注6 DNA分子演算回路
DNA鎖置換反応を連鎖させ、DNAを使ってさまざまな演算をする分子システム。鎖置換反応で放出されるDNA一本鎖を、次の鎖交換反応のインプットとして用いる。↑
注7 金属錯体型塩基対
天然の核酸塩基は、水素結合を介して塩基対を形成する。それに対し、特定の金属イオンへの結合(配位結合)を介して形成する非天然の塩基対を金属錯体型塩基対という。塩谷研究室が世界に先駆けて報告して以来、金属錯体型塩基対を形成する人工核酸塩基が多数開発されている。↑
注8 DNA分子ピンセット構造
DNA鎖の結合・解離により、開閉することができるDNAナノ構造。2000年に初めて報告され、DNA分子機械の先駆けに位置づけられる。構造的な類似性から分子ピンセットと名付けられているが、後に分子を “つかむ”ことのできるDNAナノ構造体も開発されている。 ↑
注9 デオキシリボザイム(DNAzyme)
RNA切断などの化学反応を触媒できる短鎖のDNA。DNAでできた酵素とも言える。合成が容易、かつ化学的にも安定である点が特長で、遺伝子発現制御やバイオセンシング、DNA分子機械の開発などへの応用が盛んに研究されている。 ↑
注10 相補配列
あるDNA一本鎖に対して、すべての核酸塩基がA–T, G–Cといった塩基対を形成して二重鎖をつくれる塩基配列のこと。↑


