DATE2022.06.01 #Press Releases
線虫の記憶の全貌:濃さの記憶を担うタンパク質とその情報を読みだす新たな仕組みの発見
廣木 進吾(生物科学専攻 博士課程3年生(研究当時))
飯野 雄一(生物科学専攻 教授)
発表のポイント
- 線虫(注1)という動物は、飼育されていた時の塩の濃度を記憶して、その濃度に向かって移動します。今回、この現象を利用して濃度記憶の読み出しの仕組みについて調べた結果、タンパク質のレベルから神経細胞、行動までの一連の流れの全貌が明らかになりました。
- 本研究で、記憶が味を感じる細胞の「シンタキシン」(注2)というタンパク質のリン酸化(注3)を介して書き込まれること、このリン酸化によって、移動の方向を決める神経細胞への塩濃度情報の伝わり方が反転することが明らかとなりました。
- シンタキシンはヒトを含めハエから魚類までが持つタンパク質で、今回見つかったリン酸化される部分は他の生物にも備わっています。本研究から、さまざまな生物に共通する記憶の一般的なしくみが新たに明らかになることが期待されます。
発表概要
線虫は飼育されている際のまわりの食塩の濃度を記憶し、その濃度を好むようになることが知られています。どうやって濃度を記憶して、行動に結びつけるのでしょうか。この行動のカギとなるのは、塩を感じる神経細胞であるASERだと知られています。ASER神経の中で、PKC-1というタンパク質(リン酸化酵素(注3))の働きの強さが調節されることと、強さが変わると「高い濃度に向かうか、低い濃度に行くか」が決まることまでが分かっていました。しかし、たった一つのPKC-1というタンパク質の働きが、なぜ行動の反対方向への切り替えを引き起こすことができるのかは謎でした。
今回、東京大学理学系研究科生物科学専攻 博士課程(研究当時)の廣木 進吾を中心とする研究グループは、まず、PKC-1が働くことで最終的に「シンタキシン」というタンパク質のリン酸化量が変化することを見つけました。これが、ASER神経において常に放出されている神経伝達物質グルタミン酸の量を変化させることも分かりました。このベースライン(基底状態)の放出量が変わると、ASERから信号を受け取り線虫の移動方向を制御するAIBという神経細胞で働く受容体(グルタミン酸を受け取るタンパク質)が切り替わることが分かりました。それによって、塩の濃度勾配上で線虫が塩の濃度変化を感じたときに、高い濃度へ移動するか、低い濃度に移動するかが決定されるという仕組みです。
本研究の成果と先行研究を合わせることで、記憶の分子レベルでの詳細な仕組みから行動に至るまでの一連の経路が明らかになりました。その仕組みの中心をなすのは「伝達物質放出のベースラインによる、興奮性・抑制性の切り替え」という極めて新しい原理でした。
研究内容
過去の研究によって、ASER感覚神経の中のPKC-1は、飼育時の塩濃度に比べていま自分が濃度の高い場所にいるときは働きを弱く、逆に低い濃度にいるときは働きを強くすることが分かっていました。さらに、塩の濃度勾配上を移動している最中に、PKC-1の働きが強いと線虫は濃度の高いほうに向かい、働きが弱いときは濃度の低いほうに向かうことも知られていて、これが線虫をもとの飼育時の濃度へ到達させるしくみだと考えられていました。しかしながら、PKC-1の働きがどのような分子を介して、どのような細胞の中の変化を引き起こし、どのようにして神経系の情報処理が変化することで、最終的に行動が切り替わるのかは不明でした。
研究グループは、まずPKC-1の活性化が神経細胞においてどのような分子を変化させるのかを、「神経組織特異的リン酸化プロテオミクス(注4)」という技術を用いて調べました。すると、PKC-1が活性化すると、神経細胞が神経伝達物質(注5)を放出するときに使われる分子である「シンタキシン」がリン酸化されることが分かりました。CRISPR/Cas9を使ったゲノム編集(注6)によって、このリン酸化が、高濃度・低濃度のどちらに行くかを決定するのに重要であるとわかりました。次に、このリン酸化がどのように神経伝達に影響するかを調べました。線虫の神経細胞は何も感じていないときにずっと神経伝達物質を放出しているのですが、シンタキシンのリン酸化はASERからずっと放出されている神経伝達物質グルタミン酸の放出量、すなわち「グルタミン酸のベースライン量」を変化させることが分かりました。
さらに、線虫が塩の濃度勾配上を移動する中で、このベースライン量が変わることによって、高い濃度に向かうか低い濃度に向かうかが切り替わるメカニズムを調べました。ここで着目したのが、線虫の方向転換を制御するAIBという神経細胞です。線虫が塩の濃度変化を受けたとき、ASER神経細胞が活動し、ASERからのグルタミン酸の放出量が一過的に高くなります。この変化にAIBのグルタミン酸受容体が反応し、AIBが応答します。つまり、ASERからAIBに塩濃度変化の情報が伝わり、それに従って方向転換の確率が変わることで、最終的に線虫の移動方向が適切に制御されるということになります。
以上の知見を踏まえて実験を行ったところ、「ベースラインの量」に応じて、ASERからAIBへのグルタミン酸による情報伝達が興奮性(ASERが活動するとAIBが活動する)⇔抑制性(ASERが活動するとAIBの活動が抑えられる)と切り替わることが明らかとなりました。その主な理由は、抑制性の受容体が興奮性の受容体に比べてグルタミン酸に対し反応しやすいためであることが分かりました(図1)。
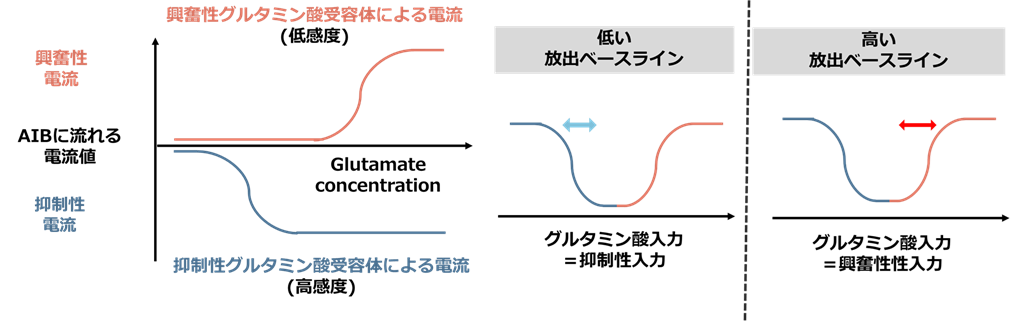
図1:ベースライン変化による興奮性・抑制性の切り替え
線虫のグルタミン酸受容体はイオンを通す「ゲート」のようになっている。抑制性受容体が開くと負の電荷をもつ陰イオンを細胞の中に通し、興奮性受容体が開くと正の電荷をもつ陽イオンを細胞の中に通す。AIB神経細胞の抑制性受容体は、興奮性受容体よりも低い濃度で完全に開く。興奮性受容体はより高い濃度のグルタミン酸がないと開かない。ベースラインが低いときは抑制性受容体のみが開くため、ASERからのグルタミン酸が一過的に増加すると、AIBの中の陰イオンが増え、AIBの活動が抑えられる。逆にベースラインが高いと、抑制性受容体は既に開ききっていて、グルタミン酸量がそれ以上増えても陰イオンは増えない。一方で、興奮性受容体は開ききってはいないため、グルタミン酸量が増えれば陽イオンが入り、AIBが活動する。
ベースラインが低いときは、興奮性受容体は反応しにくく抑制性受容体は反応しやすいので、ASERからのグルタミン酸量増加に対しAIBは抑制されます。逆にベースラインが高いときは、抑制性受容体は反応し易すぎるために飽和しており、グルタミン酸量が増加しても抑制性の反応はしなくなります。一方で、興奮性受容体はこのようなグルタミン酸量の範囲でよく応答します。そのため、今度はASERからのグルタミン酸量増加に対し興奮性の応答が見られます。
上記で明らかにされた仕組みと過去の知見を踏まえると、線虫が過去の濃度を覚える仕組みは次のように説明されます(図2)。①まず、高塩濃度・低塩濃度の飼育プレートから線虫が塩濃度勾配上に移されると、PKC-1の働きが強く/弱くなります。②それによって、シンタキシンのリン酸化レベルが変化し、最終的にグルタミン酸放出量のベースラインが増減します。③その状態で、線虫が塩の濃度勾配上を動き回ります。仮に濃度の低い側に移動したとしますと、味覚感覚神経ASERは塩の濃度が下がった時に活性化する細胞なので、ASERの活性化に伴いグルタミン酸の放出量が一過的にベースラインよりも増えます。④このときベースラインが高ければ、グルタミン酸の一過的な増加はAIBを興奮させます。AIBが興奮すると方向転換が起きるので、今度は濃度の高い側に移動することになります。逆にベースラインが低ければAIBが抑制されて、線虫がまっすぐ進むので、最終的に線虫は濃度の低い側に移動します。
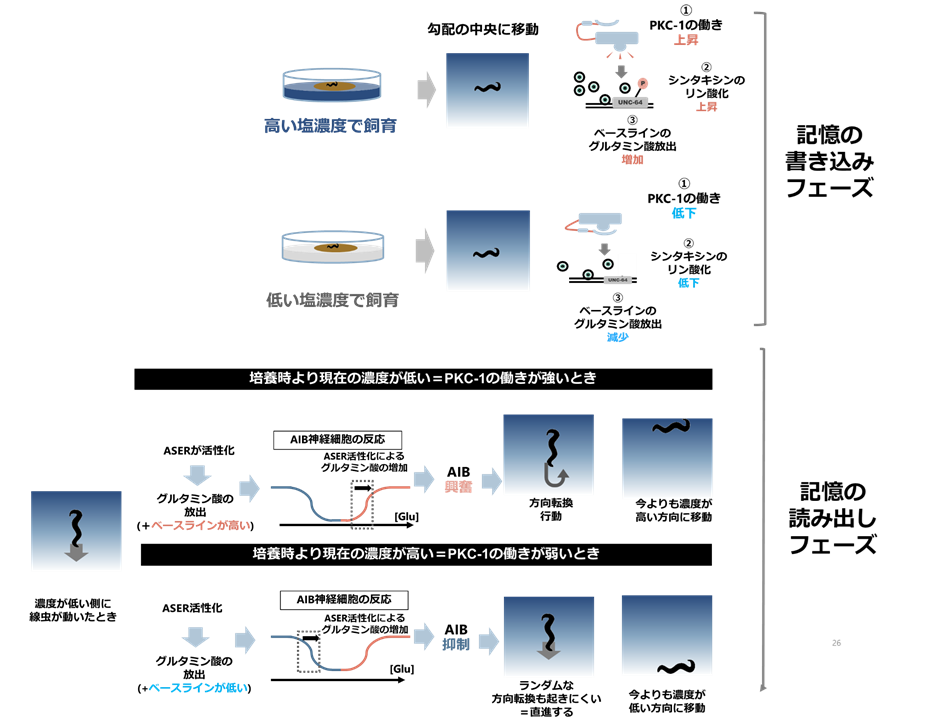
図2:本研究で明らかになった、線虫が塩の濃度を覚えるメカニズム
(上段)
飼育塩濃度より高いか・低いかに従って、リン酸化酵素PKC-1の働きの強弱が決まる。それによってシンタキシンのリン酸化量が変わり、ベースラインのグルタミン酸量が変わる。このようにして、「飼育塩濃度と今の塩濃度の差=ベースラインのグルタミン酸量」として、記憶がコードされる。
(下段)
まず、線虫は勾配上をある程度ランダムに動く。たまたま線虫が濃度の低い側に移動したときを考える。濃度が下がるとASER神経細胞が活動し、グルタミン酸の放出が一過的にベースラインよりも増える。ベースラインのグルタミン酸量が多いときは、この一過的な増加がAIB神経の活動を高める(図1参照)。AIB神経が活動すると方向転換行動が引き起こされるので、濃度の低い側に移動すると方向転換する=濃度の高い側に線虫が移動する。逆に、ベースラインのグルタミン酸量が低い時には、一過的なグルタミン酸の増加がAIB神経の活動を抑える。これによって、ランダムな方向転換が抑えられ、線虫は濃度の低い側に向かって直進しやすくなる。
このようにして、「飼育塩濃度と今の塩濃度の差=ベースラインのグルタミン酸量」が、線虫が現在よりも高い濃度・低い濃度のどちらに移動するかが決まる。
本研究によって、C. elegansという生物の記憶システムの分子から行動までの一連の流れ全体が明らかになりました。これによって、ベースライン放出による興奮性・抑制性の切り替えという新たな学習の仕組みが明らかになりました。ヒト、ハエ、魚類などはシンタキシンに相当する遺伝子を持っており、今回発見されたリン酸化を受ける場所も良く保存されています。また、ヒトを含む哺乳類の感覚神経細胞では、ベースラインの放出レベルがよく変化することが知られています。本研究によって明らかにされた新しく巧妙な仕組みは、多くの動物に共通するものかもしれません。
発表雑誌
-
雑誌名 Nature Communications 論文タイトル Molecular encoding and synaptic decoding of the context during salt chemotaxis in C. elegans 著者 Shingo Hiroki, Hikari Yoshitane, Hinako Mitsui, Hirofumi Sato, Chie Umatani, Shinji Kanda, Yoshitaka Fukada, and Yuichi Iino. DOI番号
用語解説
注1 線虫
回虫や蟯虫の仲間です。今回研究に用いた線虫は、学名「カエノラブディティス・エレガンス/C. elegans」と呼ばれる体長1mm程度の小さな生き物であり、非寄生性のため土壌や腐った果実の中で暮らしています。分子生物学や神経生物学(記憶のしくみなど)の研究に頻繁に用いられています。↑
注2 シンタキシン
神経伝達物質が神経細胞から放出されるとき、神経細胞は膜で囲まれた「シナプス小胞」という膜で囲まれた構造の中に入っています。シナプス小胞上のタンパク質(v-SNARE)が細胞膜上のタンパク質(t-SNARE)とくっつくと、小胞が細胞膜と融合し、結果としてシナプス小胞の中の神経伝達物質が外に出ます。この時に働くt-SNAREタンパク質がシンタキシンです。 ↑
注3 リン酸化・リン酸化酵素
タンパク質にはしばしば「リン酸基」と呼ばれる化合物がくっつきます。この「リン酸基」というものがつくことにより、タンパク質のかたちが変化し、その働きが大きく変化します。リン酸基がくっつくことを「リン酸化」、他のタンパク質にリン酸基をくっつける作用があるタンパク質を「リン酸化酵素」と言います。このリン酸化酵素にはたくさんのタイプがありますが、中でも非常に有名な種類の一つがPKC(プロテインキナーゼC)です。PKC-1はPKCの仲間であり、より細かい分類方法ではPKCεと呼ばれる分類に当たります。 ↑
注4 神経組織特異的リン酸化プロテオミクス
現在、技術の発展によって生物のさまざまな分子を一度に計測できるようになりました。こうした技術を用いてある種の分子群を網羅的に計測することを「オミクス解析」といい、「リン酸化プロテオミクス」とは生体内のすべてのタンパク質が、どのようにリン酸化されているかを一度に計測する手法です。これによって、PKC-1の働きによってリン酸化が増えるすべてのタンパク質を一度に調べることができます。さらに、本研究ではさらに的を絞るため、新しい技術を使い、神経細胞のタンパク質だけを抽出してきました。これをもちいて神経細胞全体のリン酸化パターンを調べる解析が「神経組織特異的リン酸化プロテオミクス」であり、本研究ではこれによってPKC-1による神経系のリン酸化の変化すべてを観察し、シンタキシンのリン酸化がみつかりました。 ↑
注5 神経伝達物質
神経細胞が隣の神経細胞に情報を伝えるときに使われる物質。脳はたくさんの神経細胞が網目状につながってできていて、つながった神経の間では一方の神経が神経伝達物質を放出し、他方の神経がそれを受け取るというバトンリレーによって情報が伝えられています。神経伝達物質にはグルタミン酸、アセチルコリン、ドーパミンなどが知られています。 ↑
注6 CRISPR/Cas9によるゲノム編集
Cas9はDNAを切断する酵素で、共に働くguideRNAと同じ配列を持つDNAを切断します。このことから、狙ったDNA配列を切らせることができ、人為的な遺伝子操作に使われます。さらには、合成DNAをこれと共に用いることにより、ゲノム上の配列を任意な配列に書き換えることができます。この技術の開発に対して2020年にノーベル化学賞が与えられました。 ↑


