DATE2022.04.15 #Press Releases
核還元のスーパー触媒 水素社会にも貢献
小林 修(化学専攻 教授)
宮村 浩之(化学専攻 助教)
発表のポイント
- 芳香環類の水素化反応は、水素の貯蔵・輸送及び、ファインケミカルズ(医薬品・化成品・農薬などの精密化学品)の製造にも適用可能な重要な反応である。今回、本反応のため、新たに開発した協調触媒系が、従来法に比べ最大でおよそ30倍の反応加速効果を示すことを見出した。
- 本研究では、不均一系金属ナノ粒子とLewis酸の協調触媒系を用いることで、大幅な反応速度の向上や新しい反応性の発現を発見し、不均一系金属ナノ粒子触媒を用いる協調触媒の新たな可能性の開拓につながる。
- 従来法では特に水素化反応が難しかった、立体的に込み入った複数の置換基を有する芳香族化合物や、かさ高く電子豊富な芳香族化合物に対して、本触媒系は特に高い活性を示した。また、従来法では高温高圧条件といった過酷な条件を必要とする、複雑で嵩高い置換基を有する芳香族化合物の立体選択的な水素化反応にも高い活性、選択性を示し、医薬品原体の原料となるビルディングブロックの合成も行った。本系は、高効率的な有用物質供給に新たな手法を提供できると期待される。
発表概要
ベンゼンなどの芳香環類の水素化反応は、水素貯蔵・輸送に応用可能で、医薬品および生理活性物質などの機能性分子の合成にとっても重要な反応である。本研究では、安価な有機―無機ハイブリッド担体を用いた、不均一ロジウム-白金二元金属ナノ粒子触媒と、水やアルコール系溶媒に安定なLewis酸であるスカンジウムトリフラートやイッテリビウムトリフラートからなる協調触媒系を開発し、芳香環類の水素化反応に適用した。この触媒系は、温和な条件下で機能し、従来法では特に水素化反応が難しかった、立体的に込み入った複数の置換基を有する芳香族化合物や、かさ高く電子豊富な芳香族化合物に対して使用可能であった。今回、本協調触媒系が、従来法に比べ最大でおよそ30倍の反応加速効果を示すことを見出した。また、従来法では高温高圧条件といった過酷な条件を必要とする、複雑で嵩高い置換基を有する芳香族化合物の立体選択的な水素化反応にも高い活性、選択性を示し、医薬品原体合成のためのビルディングブロックの合成も行った。これらの成果は高効率的な有用物質供給に新たな手法を提供できると言える。
本手法では、キラルスカンジウム錯体をポリスチレン骨格に固定化し、遠心分離操作のみで生成物、触媒、水を分離可能にした。メソエポキシドの不斉開環反応では触媒と水を10回再使用することができ、多くの医薬品に見られるキラル1,2-アミノアルコールを効率的に得ることに成功した。また、チオールの不斉1,4-付加反応、ホルマリンを用いる不斉向山アルドール反応にも応用することができた。
本研究成果は、ドイツの化学雑誌「Angewandte Chemie」および「Angewandte Chemie Internationl Edition」のオンライン速報版で日本時間4月15日午前0時(独国時間4月14日午後5時)に公開された。本研究は、文部科学省科学研究費助成事業(MEXT)の学術変革領域研究B(低エントロピー反応空間が実現する高秩序触媒化学)の計画研究の一環として行われた。
発表内容
研究の背景
水素はクリーンなエネルギー源として近年注目を集めており、医薬品・化成品・農薬などの精密化学品(ファインケミカルズ)を供給する有機合成化学の分野においても、その有効な活用法が期待されている。中でも、芳香環類またはヘテロ原子を含む芳香環類の水素化反応は、ファインケミカル合成だけでなく、有機ハイドライド法(注1)を用いた水素貯蔵および輸送を指向した応用へも活用可能であるため、水素社会への移行を実現する上でも、重要な反応である。
医薬品などさまざまな機能を有する複雑な化合物中には、さまざまな置換基を有し、立体的に込み入った脂環式部位や、ヘテロ環式部位がしばしば現れ、それらを対応する芳香族化合物の水素化反応によって合成することが、最も有効な手法の一つである。しかし、嵩高い置換基を複数有する芳香族化合物や、かさ高く電子豊富な芳香族化合物の水素化は困難で、高温高圧といった過酷な反応条件を必要とし、その効率的な合成法の開拓が課題であった。アニリン誘導体の水素化反応は、窒素を置換基に有する脂環式の化合物を与え、それらはしばしば医薬品原体等の生物活性物質の合成中間体として見いだされる。しかし、嵩高いアニリン誘導体、たとえばN,N-ジメチルアニリンの水素化反応は従来法では、20気圧水素、80 ℃以上といった過酷な反応条件を必要とし、温和な条件で機能する、より効率的な触媒系が求められていた。また、含窒素芳香族化合物であるエチルニコチネートの水素化体は医薬品原体合成の中間体を与えることから、その触媒的水素化反応が広く研究されているが、その部分水素化体の安定性ゆえ、飽和水素化体を得るためには、高温高圧条件を必要としていた。
一方、複数の触媒で別々の基質をそれぞれ活性化する協調触媒系は、相乗的に遷移状態の活性化エネルギーを低減化できることから、温和な反応条件下、少ない触媒量をもって、高難易度の反応を進行させることが可能で、省エネルギー、省物質といったSDGs達成においても注目を集めている。しかしながら、このような協調触媒系は主に均一系触媒で開発がさかんに行われており、回収、再使用が可能で、一層の省資源、省物質を可能とする不均一系触媒における協調触媒系の開発はいまだ発展途上であった。
研究の内容
本研究では、まずN,N-ジメチルアニリンやオルトキシレンといった、かさ高い置換基を複数有する芳香族化合物の水素化反応に有効な、協調触媒系の開発を行った。これまで独自に開発してきた、入手容易な有機―無機ハイブリッド担体に担持したロジウムー白金(Rh-Pt)二元ナノ粒子触媒は、トルエンの水素化反応において、常温常圧といった温和な条件下非常に高い触媒活性を示していたが、かさ高い置換基を複数有する芳香族化合物の水素化反応には高温高圧条件を必要としていた。そこで本研究では、不均一系金属ナノ粒子とLewis酸の協調触媒系を用いることで、Lewis酸を添加しない場合には水素化が困難な基質に対しても、大幅な反応速度の向上を見出し、いずれの場合も反応温度40-50 ℃、大気圧水素という温和な条件下、高い収率で芳香族化合物の水素化反応が進行することを見出した(図1)。

図1:Rh-Ptナノ粒子触媒とLewis酸触媒からなる協調触媒系を用いる芳香族化合物の 水素化反応
本協調触媒系についての反応機構研究のため、反応速度論解析や、核磁気共鳴装置(NMR)を用いる検討を行った結果、Lewis酸は基質と液相中で直接相互作用し、その複合体が、不均一系触媒表面で活性化された水素と反応することで、円滑に反応が進行していることが示唆された。また、オルトキシレンの水素化反応における反応速度論解析の結果、1.25 mol%のスカンジウムトリフラートを添加することで、30倍以上の反応加速が観測され、顕著なLewis酸による反応加速効果が確認された。
本触媒系は、炭化水素系芳香族化合物やアニリン誘導体のみならず、複数の置換基を有するピリジン誘導体におけるジアステレオ選択的な水素化反応にも有効に機能し、その生成物はさまざまな生物活性化合物の合成中間体として用いることができる(図2)。また、置換基として、かさ高く複雑なキラル補助剤を含む芳香族化合物の水素化反応においても、高い立体選択性を示した(図3)。このようなキラル補助剤を含む芳香族化合物の水素化反応は、従来法では高温や50気圧以上の水素を用いる必要があったが、本触媒系を用いることで一気圧の水素で高い収率で目的物が得られた。
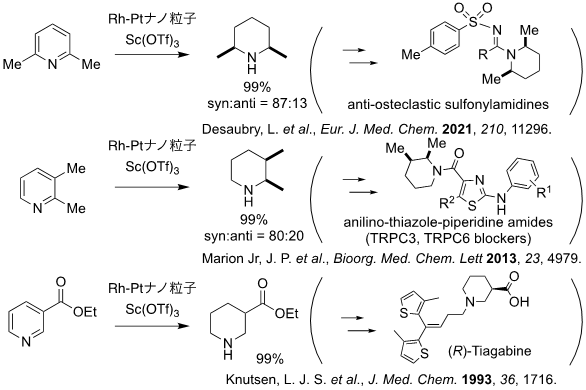
図2:本触媒系を用いる医薬品原体や生物活性化合物合成のためのビルディングブロック合成
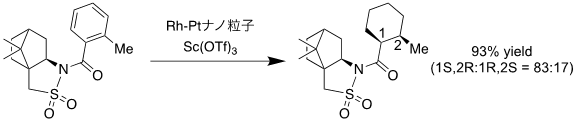
図3:本触媒系を用いるキラル補助剤を有する芳香族化合物の立体選択的水素化反応
今後の展開
本研究では、芳香環水素化反応を効率的に行える、不均一系金属ナノ粒子とLewis酸触媒からなる協調触媒系の開発を行った。本触媒系を用いることで、これまで水素化反応において過酷な反応条件を必要とした高難度な基質においても温和な条件下での円滑な反応を実現できたことにより、水素を基軸としたさまざまなプロセスの省エネルギー化や省資源化の加速が期待される。また選択的水素化の知見を元に、ファインケミカルズのより効率的な合成ルートを開拓できると考えられる。
発表雑誌
-
雑誌名 Angewandte Chemie , Angewandte Chemie International Edition 論文タイトル Reaction Rate Acceleration of Cooperative Catalytic Systems: Metal Nanoparticles and Lewis Acids in Arene Hydrogenation 著者 Hiroyuki Miyamura *, and Shū Kobayashi * DOI番号
用語解説
注1 有機ハイドライド法
芳香族炭化水素とその水素化体を媒介にして水素の貯蔵や輸送に活用する方法。水素は気体であるため取り扱いが難しく、貯蔵や輸送に問題が生じる。ベンゼン、トルエン、ナフタレンなどの芳香族炭化水素を水素化し、水素を有機分子中に固定化すれば、安定な液体として貯蔵・輸送することができる。逆反応である脱水素化反応を行えば、必要な場所で水素を取り出せると同時に、芳香族炭化水素が再生し再利用が可能である。↑


