DATE2025.09.22 #Press Releases
タンパク質複合体構造の進化の歴史は繰り返す
―大規模ゲノム情報からの偶然の発見をもとに実験で証明―
発表のポイント
- 2万種以上の細菌ゲノムの情報解析により、アルコール代謝の二段階の反応を担う酵素遺伝子が融合して誕生した二機能性酵素(BdhE)を新規に発見しました。さらに生化学・構造生物学実験により、この融合酵素の触媒効率を向上すると考えられる立体構造が、二つの異なる系統で独立に収斂進化したことを示しました。
- これまで報告されていたタンパク質の収斂進化は特定のアミノ酸残基や局所的な立体構造のスケールに留まっていましたが、本研究ではより大きなタンパク質複合体スケールで、進化の歴史が繰り返しうることを示しました。
- 本成果はタンパク質立体構造の進化のパターン・法則性の理解に繋がるのみならず、高効率なバイオエタノール生産を可能にする新規遺伝子資源の発見という点で、今後の応用研究も期待できます。
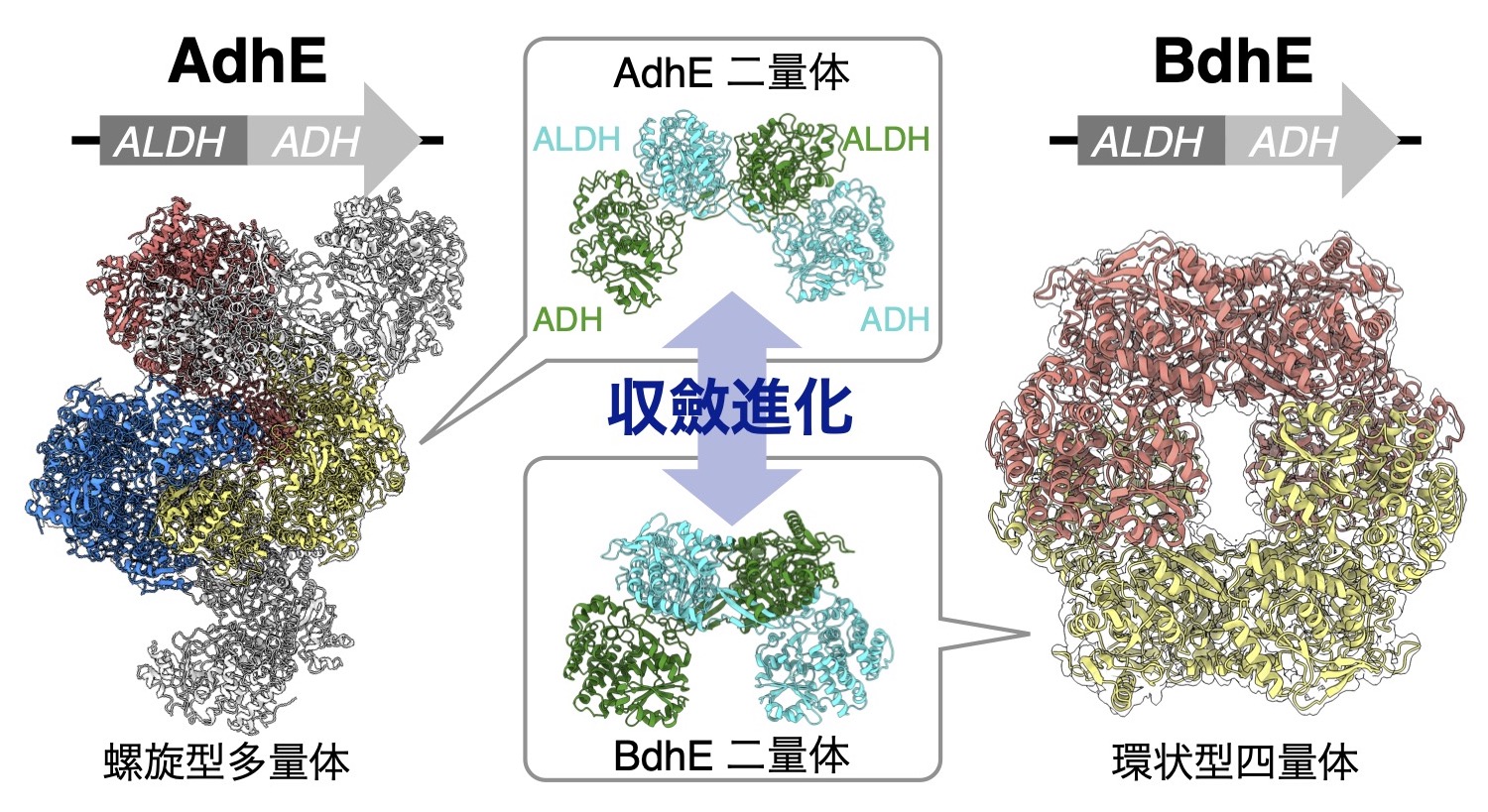
融合酵素AdhEとBdhEでは複合体構造が収斂進化している*9/22図差し替え
発表概要
東京大学大学院理学系研究科の今野直輝客員共同研究員、古澤力教授らによる研究チームは、細菌のゲノム情報からアルコール代謝に関わる新規の二機能酵素BdhEを発見し、タンパク質複合体(注1) の三次元構造が異なる2系統で収斂進化(注2) していることを明らかにしました。本研究は、2万種以上の細菌のゲノム情報解析、酵素活性測定、タンパク質立体構造解析を分野横断的に活用することで、新規遺伝子の発見とタンパク質の機能・構造解析に基づく進化の議論を可能にしました。これまでアミノ酸残基や局所的な立体構造のスケールに留まっていたタンパク質の収斂進化の研究を、タンパク質複合体のスケールへ拡張する成果です。本研究で発見した酵素はアルコール代謝の二段階反応を効率的に触媒できると考えられる構造を有し、バイオエタノール生産の代謝工学への活用も期待されます。
発表内容
進化生物学分野では自然界で過去に起きた進化の研究が広く行われていますが、過去に一度しか起きていない進化現象の背後にあるメカニズムや法則性を探ることは一般に困難です。しかし自然界では、独立な系統が共通の性質を進化させることもあり(収斂進化)、そのような「過去に繰り返し起きた進化」は、どの環境条件でどのような進化が起きやすいのかという法則性を理解する上での強力な手掛かりとして注目されてきました。多くの主要な生命機能を担う生体分子であるタンパク質についても収斂進化が研究されてきましたが、これまでの報告は特定のアミノ酸残基や局所的なタンパク質構造のスケールに留まっていました。
本研究チームは、別プロジェクトでの2万種以上の細菌のゲノム情報解析の際に、アルコール代謝に関わるアルデヒド脱水素酵素(ALDH)とアルコール脱水素酵素(ADH)が一体化してできた新規の融合酵素(BdhE; Bifunctional dehydrogenase E)を偶然に発見しました。 ALDHとADHはヒトをはじめ様々な生物が持つ酵素で、アルデヒドを介してアルコールをカルボン酸に可逆的に変換する二段階の代謝反応を触媒しますが(図1A)、BdhEは一つの酵素で両方の反応を連続的に進められます。似た融合酵素としてこれまでにAdhEが知られていましたが、AdhEとBdhEを含む進化的に近縁なタンパク質の分子系統樹を調べた結果、BdhEはAdhEとは独立な遺伝子融合によって成立したことが明らかになりました(図1B)。

図1:(A) ALDHとADHが触媒する二段階の代謝反応。 (B) AdhEとBdhEの単量体構造とAdhE、BdhEを含むALDHの分子系統樹。吹き出し内にはAdhEとBdhEの単量体の立体構造(予測構造)を示した。系統樹上の紫色の点が融合酵素(AdhEまたはBdhE)、赤色の点がALDHのみからなる酵素を表す。系統樹上の数字(%)は系統樹上の各枝の信頼度(UFBoot値)を表す。この系統樹からAdhEとBdhEが異なる系統に分かれていることが示された。
過去の研究から、AdhEではALDHとADHの間で基質化合物を効率よく受け渡せる立体構造が進化しており、触媒効率の上昇や中間生成物であるアルデヒドの毒性回避に寄与していることが示唆されていました。そこで本研究チームは、独立な遺伝子融合で誕生した類似の融合酵素AdhEとBdhEでは、その後の進化の過程で共通の選択圧のもと、類似の立体構造が収斂進化しているという仮説を立てました。検証のためにクライオ電子顕微鏡(注3) を用いたタンパク質構造解析を行ったところ、AdhEが螺旋型の多量体を形成するのに対してBdhEは環状型の四量体を形成することが判明し、一見、仮説を否定する結果が得られました(図2)。しかし詳細に構造を観察すると、螺旋型および環状型の複合体はいずれも、ALDHとADHの相互作用によって形成される二量体ユニットから成り、この構造によって中間産物のアルデヒドをALDH-ADH間で効率的に受け渡す通り道が形成されていることが示唆されました。このことから、AdhEとBdhEの類似した二量体構造は、触媒効率の向上とアルデヒドの漏出抑制(毒性回避)という共通の選択圧のもとで収斂進化したと考えられます。

図2:AdhEとBdhEの電子顕微鏡画像と決定された複合体構造。ALDH-ADH間の相互作用界面の構造(一番右)を観察すると、AdhEとBdhEは異なる部位のアミノ酸残基を使って同様の相互作用を達成していることが判明した。このことは二量体構造が収斂進化したことを裏付ける。*9/22差し替え
この成果は、これまでアミノ酸残基や局所的な立体構造のスケールの報告に留まっていたタンパク質の収斂進化が、タンパク質複合体のスケールでも起こりうることを証明し、今後タンパク質立体構造の進化の法則性を探索する研究の基盤となります。また、共通の選択圧で収斂進化が起きると同時に、複合体構造全体は大きく異なる点(螺旋型と環状型)も興味深く、タンパク質の構造が多様化する進化メカニズムの理解にも繋がります(図3)。さらに、高効率のアルコール代謝を可能にする酵素はバイオエタノール生産の分野で注目されており、本成果はそのための新規遺伝子資源の発見として今後の研究に繋がることが期待されます。
 図3:本研究で明らかになったAdhEとBdhEの進化過程
図3:本研究で明らかになったAdhEとBdhEの進化過程
発表者・研究者等情報
東京大学 大学院理学系研究科 生物普遍性研究機構 今野 直輝(客員共同研究員)、古澤 力(教授)
論文情報
-
雑誌名 Nature Communications 論文タイトル Repeatability of protein structural evolution following convergent gene fusions著者 Naoki Konno*, Keita Miyake, Satoshi Nishino, Kimiho Omae, Haruaki Yanagisawa, Saburo Tsuru, Yuki Nishimura, Masahide Kikkawa, Chikara Furusawa, Wataru Iwasaki(*責任著者) DOI番号 10.1038/s41467-025-63898-x
研究助成
本研究は科研費(課題番号: 22J20318, 24H00870, JP22H04925, 21H05247, 21H05248)、JST(課題番号: GteX JPMJGX23B2, ERATO JPMJER1902)、The ANRI Fellowship、AMED-BINDS(課題番号: JP24ama121002)の支援により実施されました。
用語解説
注1 タンパク質複合体
複数のタンパク質分子が相互作用することで結合した状態。同じタンパク質分子からなる場合をホモ複合体、異なるタンパク質分子からなる場合をヘテロ複合体と呼ぶ。今回AdhEとBdhEで観察されたのはどちらもホモ複合体である。↑
注2 収斂進化
異なる複数の系統で共通の性質が進化する現象。背後の進化メカニズムを理解する手掛かりになる。↑
注3 クライオ電子顕微鏡
タンパク質構造をはじめとする微小構造を観察可能な顕微鏡。タンパク質の立体構造解析に広く用いられている。↑


