DATE2023.01.10 #プレスリリース
リボソームの異常な交通渋滞を選別するしくみを解明
――高速AFMを用いて品質管理を司る複合体の動きを可視化――
東京大学
名古屋大学
自然科学研究機構生命創成探究センター
科学技術振興機構
発表概要
東京大学医科学研究所RNA制御学分野の松尾芳隆准教授、稲田利文教授(大学院新領域創成科学研究科/大学院理学系研究科生物科学専攻兼担)らの研究グループは、名古屋大学理学研究科の内橋貴之教授(自然科学研究機構生命創成探究センター客員教授兼任)と共同でリボソームの異常な交通渋滞を選別するしくみを解明しました。
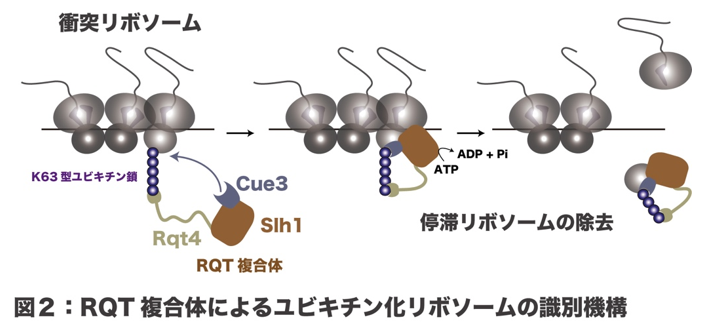
リボソームは、mRNAの遺伝情報を読み取ってタンパク質を合成する「翻訳」を行なう装置であり、翻訳を停止したリボソームに後続のリボソームが衝突することによってリボソームの交通渋滞が起こります。細胞内でリボソームの交通渋滞が蓄積すると様々なストレス応答が誘導されます。一方で過剰なストレス応答を防ぐために、細胞はリボソームの交通渋滞を解消する品質管理機構を備えています。品質管理因子であるHel2はリボソームの衝突を識別し、異常翻訳の目印としてユビキチンを付加します。このユビキチン化が目印となり、RQT(Ribosome Quality control Trigger)複合体が衝突リボソームを強制的にサブユニット解離させることで交通渋滞を解消します。リボソームのユビキチン化は衝突リボソームの除去に必須ですが、それを識別する分子機構は十分に理解されていませんでした。
本研究グループは、生化学的手法を用いて衝突リボソームにK63型のユビキチン鎖が形成され、それをRQT複合体の構成タンパク質であるCue3とRqt4が識別することを発見しました。さらに、1分子レベルの動態を可視化できる高速AFMを用いて、RQT複合体の動き、特に運動性の高い天然変性領域の可視化に成功しました。
本成果は、品質管理機構の破綻が原因とされる神経変性疾患などの発症機序の理解や新規治療戦略の開発に繋がることが期待されます。
本研究は、科学技術振興機構(JST)戦略的創造研究推進事業さきがけ“細胞の動的高次構造体”領域(課題番号:JPMJPR21EE、研究代表者:松尾芳隆)、日本学術振興会科学研究費助成事業(課題番号:21H00267、21H05710、22H02606、松尾芳隆; 21H01772、21H00393、内橋貴之;19H05281、21H05277、22H00401、稲田利文)、日本医療研究開発機構(AMED-CREST 課題番号:20gm1110010h0002、研究代表者:稲田利文)などの支援を受けて行われました。
本研究成果は2023年1月10日(火)午後7時(イギリス時間10日午前10時)、英国科学誌「Nature Communications」のオンライン版で公開されました。
詳しくは、東京大学医科学研究所 のホームページをご覧ください。


